Kontakt:Errol Zhou (MR.)
Tlf: pluss 86-551-65523315
Mobil/WhatsApp: pluss 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-post:sales@homesunshinepharma.com
Legg til:1002, Huanmao Bygning, Nr.105, Mengcheng Vei, Hefei By, 230061, Kina
Gilead og dets partner Galapagos NV kunngjorde nylig at EU-kommisjonen (EF) har godkjent Jyseleca (filgotinib, 200 mg og 100 mg tabletter), som er en oral selektiv JAK1-hemmer for behandling av voksne pasienter med moderat til alvorlig revmatoid artritt (RA) med utilstrekkelig respons eller intoleranse mot flere sykdomsmodifiserende antireumatiske legemidler (DMARD). Når det gjelder medisiner, kan Jyseleca brukes som monoterapi eller i kombinasjon med metotreksat (MTX).
Samme dag kunngjorde Gilead og Eisai i fellesskap at departementet for helse, arbeid og velferd (MHLW) i Japan har godkjent Jyseleca (200 mg og 100 mg tabletter) for behandling av RA-pasienter som ikke responderer på konvensjonell behandling, inkludert forebygging. av strukturelle leddskader. I henhold til samarbeidsavtalen som ble inngått i desember 2019, har Gilead Japan salgslisensen til Jyseleca i Japan, og Eisai vil være ansvarlig for distribusjonen av legemidlet i Japan for behandling av RA og andre potensielle fremtidige indikasjoner, inkludert ulcerøs kolonbetennelse, Crohns sykdom, psoriasisartritt, etc.
Det er verdt å merke seg at når det gjelder amerikansk regulering, utstedte FDA et komplett svarbrev (CRL) i august i år, og nektet å godkjenne Jyseleca. FDA har bedt om data fra MANTA- og MANTA-RAy-studiene. Disse to studiene har nå fullført pasientrekruttering for å vurdere om filgotinib har en effekt på sædparametere. Resultatene fra topplinjen forventes å bli kunngjort i første halvdel av 2021. I tillegg har FDA også uttrykt bekymring for filgotinibs samlede fordel / risikoprofil i en dose på 200 mg. Da Nead ble sendt til FDA i desember 2019, brukte Gilead en Priority Review Voucher (PRV) for å øke hastigheten på gjennomgangen. Denne PRV ble kjøpt av Gilead fra Ultragenyx for $ 80 millioner. CRL betyr også at 80 millioner amerikanske dollar er forgjeves.
Revmatoid artritt (RA) er en kronisk, progressiv, systemisk og inflammatorisk sykdom som kan forårsake alvorlig og irreversibel leddestruksjon, smerte og funksjonsnedsettelse. Det er nesten 3 millioner RA-pasienter i Europa, hvorav mange ikke kan oppnå langvarig symptomkontroll, noe som vil føre til hyppigere symptomutbrudd og sykdomsprogresjon, noe som alvorlig påvirker livskvaliteten. Selv om det er tilgjengelige behandlinger, er det fortsatt behov for nye behandlinger for å gi pasienter effektiv symptomkontroll og hjelpe til med å håndtere innvirkningen av RA på pasienter' hverdagen på den beste måten.
Jyseleca er en ny JAK-hemmer som har jevn sikkerhet gjennom hele det kliniske utviklingsprosjektet og har vist sterk symptomkontroll og sykdomsforebygging. Data fra kliniske studier viser at Jyseleca har vist klinisk forbedring, lav sykdomsaktivitet og klinisk remisjon i en bred pasientpopulasjon (inkludert pasienter med utilstrekkelig respons på biologiske midler). Godkjenningen av legemidlet vil gi et nytt og populært valg for RA-pasientgrupper i Europa og Japan.
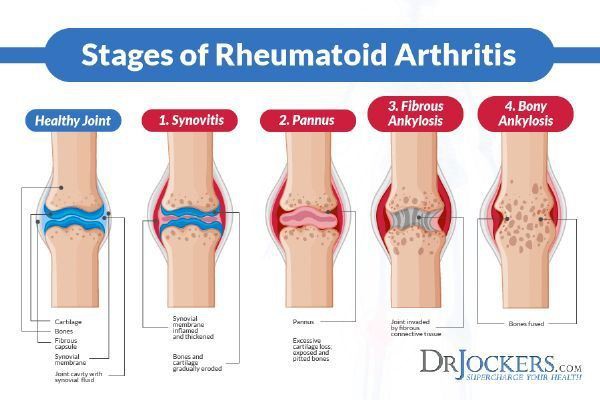
Revmatoid artritt (RA, bildekilde: drjockers.com)
Jyseleca ble godkjent i EU og Japan, basert på data fra fase III FINCH og fase II DARWIN-prosjektene. Mer enn 3.500 pasienter i disse prosjektene fikk Jyseleca-behandling, inkludert nybehandlede pasienter og pasienter med utilstrekkelig respons på biologiske DMARDs. FINCH-prosjektet inkluderer 3 fase III-studier som involverer et bredt spekter av RA-pasienter, og alle 3 studiene nådde sine primære endepunkter. I studien nådde Jyseleca konsekvent ACR20 / 50/70-indeksen, og sammenlignet med placebo eller MTX viste alle individuelle ACR-komponenter forbedring.
Sammenlignet med placebo eller MTX oppnådde pasienter som fikk Jyseleca 200 mg kombinert med MTX eller andre konvensjonelle syntetiske sykdomsmodifiserende antireumatiske legemidler (csDMARD) i 12. og 24. uke lav sykdomsaktivitet og / eller sykdomsremisjon (Andelen pasienter med DAS28 -CRP≤3.2 og DAS28-CRP < 2.6) var signifikant høyere.
Hos pasienter med utilstrekkelig respons på MTX ble den modifiserte totale Sharp-poengsummen (mTSS) brukt i den 24. uken. Sammenlignet med placebo + MTX, hadde Jyseleca + MTX-behandling en statistisk signifikant hemmende effekt på utviklingen av strukturell leddskade. I DARWIN 3 fase II åpen, langvarig forlengelsesstudie hos pasienter som får Jyseleca 200 mg monoterapi eller kombinert med MTX, kan den langvarige responsen på ACR20 / 50/70 opprettholdes i opptil tre år.
I FINCH- og DARWIN-prosjektforsøkene var de fire vanligste bivirkningene kvalme, infeksjon i øvre luftveier, urinveisinfeksjon og svimmelhet. Forekomsten av helvetesild og lungebetennelse er uvanlig. Forekomsten av alvorlige infeksjoner var 1,0% i Jyseleca 200 mg-gruppen og 0,6% i placebogruppen. I den omfattende sikkerhetsanalysen av 7 kliniske studier var forekomsten av store bivirkninger (MACE) og venøs tromboembolisme (VTE) i Jyseleca sammenlignbar med placebo. Ved langvarig medisinering forblir forekomsten av alvorlige infeksjoner stabil.

Molekylær struktur av filgotinib (bildekilde: Wikipedia)
Den aktive farmasøytiske ingrediensen i Jyseleca er filgotinib, som er en svært selektiv JAK1-hemmer, oppdaget og utviklet av Galapagos. I slutten av desember 2015 nådde Gilead en avtale med Galapagos for et samlet beløp på opptil 2 milliarder amerikanske dollar for å utvikle filgotinib i fellesskap. Dette samarbeidet vil bidra til å styrke Gileads posisjon innen inflammatoriske sykdommer, som også vil bli et nytt vekstpunkt for Gilead i fremtiden etter hepatitt C og HIV.
For tiden gjennomfører Gilead og Galapagos en rekke studier for å evaluere potensialet til Jyseleca for å behandle en rekke inflammatoriske sykdommer. Fase III-studier inkluderer behandling av revmatoid artritt, Crohns sykdom og ulcerøs kolitt. EvaluatePharma, en farmasøytisk markedsundersøkelsesorganisasjon, ga tidligere ut en rapport om at Jyseleca vil bli et av Gileads viktigste produkter for å fremme fremtidig vekst. I 2024 forventes det globale salget å nå 1,4 milliarder amerikanske dollar.
Men innen JAK-hemmere vil Jyseleca også møte flere konkurrerende produkter. I tillegg til de to oppførte produktene, Pfizer Xeljanz og Eli Lilly Olumiant, vil den sterkere motstanderen være AbbVie' s Rinvoq (upadacitinib). Foreløpig er Rinvoq vellykket godkjent av USA og EU for behandling av moderat til alvorlig revmatoid artritt (RA). EvaluerePharma spådde tidligere at etter at Rinvoq ble offentlig, vil salget i 2024 nå USD 2,57 milliarder dollar.